Статья посвящена врождённому и приобретённому ЭКГ-синдрому удлинённого интервала QТ, а также Амиодарону, как наиболее частой медикаментозной причине данного состояния.
Синдром удлинения QT интервала представляет собой сочетание удлиненного интервала QT стандартной ЭКГ и угрожающих жизни полиморфных желудочковых тахикардий (torsade de pointes - «пируэт»). Пароксизмы желудочковых тахикардий типа «пируэт» клинически проявляются эпизодами потери сознания и нередко заканчиваются фибрилляцией желудочков, являющихся непосредственной причиной внезапной смерти.
Длительность интервала QT зависит от частоты сердечных сокращений и пола пациента. Поэтому используют не абсолютную, а корригированную величину интервала QT (QTc), которую рассчитывают по формуле Базетта:
где: RR - расстояние между соседними зубцами R на ЭКГ в сек. ;
К = 0, 37 для мужчин и К = 0, 40 для женщин.
Удлинение интервала QT диагностируют в том случае, если длительность QTc превышает 0, 44 с.
Установлено, что как врожденные, так и приобретенные формы удлинения интервала QT являются предикторами фатальных нарушений ритма, которые, в свою очередь, приводят к внезапной смерти больных.
В последние годы большое внимание уделяется изучению вариабельности (дисперсии) величины QT интервала - маркера негомогенности процессов реполяризации, поскольку увеличенная дисперсия интервала QT также является предиктором развития ряда серьезных нарушений ритма, включая внезапную смерть. Дисперсия QT интервала - это разница между максимальными и минимальными значениями QT интервала, измеренного в 12 стандартных отведениях ЭКГ: Д QT = QTmax- QTmin.
Так, отсутствует единое мнение о верхней границе нормальных значениях дисперсии корригированного интервала QT. По мнению одних авторов, предиктором желудочковых тахиаритимий является QTcd более 45, другие исследователи предлагают считать верхней границей нормы QTcd 70 мс и даже 125 мс.
Cуществуют два наиболее изученных патогенетических механизма аритмий при синдроме удлиненного QT интервала. Первый - механизм «внутрисердечных нарушений» реполяризации миокарда, а именно, повышенная чувствительность миокарда к аритмогенному эффекту катехоламинов. Второй патофизиологический механизм - дисбаланс симпатической иннервации (снижение правосторонней симпатической иннервации вследствие слабости или недоразвития правого звездчатого ганглия). Эта концепция подтверждается на моделях с животными (удлинение QT интервала после правосторонней стеллэктомии) и результатами левосторонней стеллэктомии в лечении резистентных форм удлинения QT интервала.
Частота выявления удлинения интервала QT у лиц с пролапсами митрального и/или трикуспидального клапанов достигает 33%. По мнению большинства исследователей, пролапс митрального клапана является одним из проявлений врожденной дисплазии соединительной ткани. Среди других проявлений «слабости соединительной ткани» - повышенная растяжимость кожи, астенический тип телосложения, воронкообразная деформация грудной клетки, сколиоз, плоскостопие, синдром гипермобильности суставов, миопия, варикозное расширение вен, грыжи. Рядом исследователей выявлена взаимосвязь увеличенной варибельности QT интервала и глубины пролабирования и/или наличия структурных изменений (миксоматозная дегенерация) створок митрального клапана. Одной из главных причин формирования удлинения интервала QT у лиц с пролапсом митрального клапана является генетически предопределенный или приобретенный дефицит магния
Приобретенное удлинение QT интервала может возникнуть при атеросклеротическом или постинфарктном кардиосклерозе, при кардиомиопатии, на фоне и после перенесенного мио- или перикардита. Увеличение дисперсии интервала QT (более 47 мс) может также являться предиктором развития аритмогенных синкопальных состояний у больных с аортальными пороками сердца.
Удлинение интервала QT может наблюдаться и при синусовой брадикардии, атриовентрикулярной блокаде, хронической цереброваскулярной недостаточности и опухоли головного мозга. Острые случаи удлинения интервала QT могут также возникать при травмах (грудной клетки, черепно-мозговых).
Автономная нейропатия также увеличивает величину интервала QT и его дисперсию, поэтому данные синдромы имеют место у больных сахарным диабетом I и II типов.
Удлинение интервала QT может иметь место при нарушениях электролитного баланса с гипокалиемией, гипокальциемией, гипомагнезиемией. Подобные состояния возникают под воздействием многих причин, например, при длительном приеме диуретиков, особенно петлевых (фуросемид). Описано развитие желудочковой тахикардии типа «пируэт» на фоне удлинения интервала QT cо смертельным исходом у женщин, находившихся на малобелковой диете с целью снижения массы тела.
Общеизвестно удлинение QT при острой ишемии миокарда и инфаркте миокарда. Стойкое (более 5 дней) увеличение интервала QT, особенно при сочетании с ранними желудочковыми экстрасистолами, прогностически неблагоприятно. У этих пациентов выявлено значительное (в 5-6 раз) повышение риска внезапной смерти.
В патогенезе удлинения QT при остром инфаркте миокарда, несомненно, играет роль гиперсимпатикотония, именно этим многие авторы объясняют высокую эффективность b-блокаторов у этих пациентов. Кроме того, в основе развития данного синдрома лежат и электролитные нарушения, в частности, дефицит магния. Результаты многих исследований свидетельствуют о том, что до 90% больных с острым инфарктом миокарда имеют дефицит магния. Выявлена также обратная корреляционноая взаимосвязь уровня магния в крови (сыворотке и эритроцитах) с величиной интервала QT и его дисперсией у пациентов с острым инфарктом миокарда.
У пациентов с идиопатическим пролапсом митрального клапана лечение следует начинать с применения пероральных препаратов магния (Магнерот по 2 табл. 3 раза в день в течение не менее 6 месяцев), поскольку тканевой дефицит магния считают одним из основных патофизиологических механизмов формирования как синдрома удлинения QT интервала, так и «слабости» соединительной ткани. У этих лиц после лечения препаратами магния не только нормализуется величина интервала QT, но и уменьшаются глубина пролабирования створок митрального клапана, частота желудочковых экстрасистол, выраженность клинических проявлений (синдрома вегетативной дистонии, геморрагических симптомов и др.). Если лечение пероральными препаратами магния через 6 месяцев не оказало полного эффекта показано добавление b-блокаторов.
Другой важной причной удлинёния интервала QT является приём специальных медикаментов, одним из таких препаратов, чаще всего используемых в клинической практике является Амиодарон (Кордарон).
Амиодарон относится к III классу антиаритмических препаратов (класс ингибиторов реполяризации) и обладает уникальным механизмом антиаритмического действия, так как помимо свойств антиаритмиков III класса (блокада калиевых каналов) он обладает эффектами антиаритмиков I класса (блокада натриевых каналов), антиаритмиков IV класса (блокада кальциевых каналов) и неконкурентным бета-блокирующим действием.
Кроме антиаритмического действия у него имеются антиангинальный, коронарорасширяющий, альфа- и бета-адреноблокирующий эффекты.
Антиаритмические свойства:
- увеличение продолжительности 3-ей фазы потенциала действия кардиомиоцитов, в основном за счет блокирования ионного тока в калиевых каналах (эффект антиаритмика III класса по классификации Вильямса) ;
- уменьшение автоматизма синусового узла, приводящее к уменьшению частоты сердечных сокращений;
- неконкурентная блокада альфа- и бета- адренергических рецепторов;
Описание
- замедление синоатриальной, предсердной и атриовентрикулярной проводимости, более выраженное при тахикардии;
- отсутствие изменений проводимости желудочков;
- увеличение рефрактерных периодов и уменьшение возбудимости миокарда предсердий и желудочков, а также увеличение рефрактерного периода атриовентрикулярного узла;
- замедление проведения и увеличение продолжительности рефрактерного периода в дополнительных пучках предсердно-желудочкового проведения.
Другие эффекты:
- отсутствие отрицательного инотропного действия при приеме внутрь;
- снижение потребления кислорода миокардом за счет умеренного снижения периферического сопротивления и частоты сердечных сокращений;
- увеличение коронарного кровотока за счет прямого воздействия на гладкую мускулатуру коронарных артерий;
- поддержания сердечного выброса за счет снижения давления в аорте и снижения периферического сопротивления;
- влияние на обмен тиреоидных гормонов: ингибирование превращения Тз в Т4 (блокада тироксин-5-дейодиназы) и блокирование захвата этих гормонов кардиоцитами и гепатоцитами, приводящее к ослаблению стимулирующего влияния тиреоидных гормонов на миокард.
Терапевтические эффекты наблюдаются в среднем через неделю после начала приема препарата (от нескольких дней до двух недель). После прекращения его приема амиодарон определяется в плазме крови на протяжении 9 месяцев. Следует принимать во внимание возможность сохранения фармакодинамического действия амиодарона в течение 10-30 дней после его отмены.
Каждая доза амиодарона (200 мг) содержит 75 мг йода.
Показания к применению
Профилактика рецидивов
- Угрожающих жизни желудочковых аритмий, включая желудочковую тахикардию и фибрилляцию желудочков (лечение должно быть начато в стационаре при тщательном кардиомониторном контроле).
- Наджелудочковых пароксизмальных тахикардии:
- документированных приступов рецидивирующей устойчивой наджелудочковой пароксизмальной тахикардии у больных с органическими заболеваниями сердца;
- документированных приступов рецидивирующей устойчивой наджелудочковой пароксизмальной тахикардии у больных без органических заболеваний сердца, когда антиаритмические препараты других классов не эффективны или имеются противопоказания к их применению;
- документированных приступов рецидивирующей устойчивой наджелудочковой пароксизмальной тахикардии у больных с синдромом Вольфа-Паркинсона-Уайта.
- Мерцательной аритмии (фибрилляции предсердий) и трепетания предсердий
Профилактика внезапной аритмической смерти у больных группы высокого риска
- Больные после недавно перенесенного инфаркта миокарда, имеющих более 10 желудочковых экстрасистол в 1 час, клинические проявления хронической сердечной недостаточности и сниженную фракцию выброса левого желудочка (менее 40%).
Амиодарон может использоваться при лечении нарушений ритма у пациентов с ишемической болезнью сердца и /или нарушениями функции левого желудочка
Для больных хронической сердечной недостаточностью амиодарон является единственным разрешенным к применению антиаритмиком. Это связано с тем, что прочие препараты у этой категории пациентов или увеличивают риск внезапной середечной смерти, или угнетают гемодинамику.
При наличии ишемической болезни сердца препаратом выбора является соталол, на 1/3 являющийся, как известно, b-адреноблокатором. Но при его неэффективности в нашем распоряжении вновь только амиодарон. Что же касается больных с артериальной гипертензией, то из их числа, в свою очередь, выделяются пациенты с выраженной и невыраженной гипертрофией левого желудочка. Если гипертрофия невелика (в Руководстве 2001 г. - толщина стенки левого желудочка менее 14 мм), препарат выбора - пропафенон, но при его неэффективности - как всегда, амиодарон (наряду с соталолом). Наконец, при выраженной гипертрофии левого желудочка, как и при хронической сердечной недостаточности, амиодарон - единственный возможный препарат.
То, что медикаментозная антиаритмическая терапия не дает снижения общей смертности, но частично даже приводит к повышению смертности, обусловлено риском пародоксального увеличения аритмий - то есть проаритмическим действием субстанций Vaughan-Williams-классов I и III.
Показательные результаты CAST-исследования (Cardiac Arrhytmia Supression Trial), в котором при сравнительной оценке поразительно обнаружилось, что под действием IC-антиаритмиков Flecainid и Encainid умерло больше постинфарктных пациентов, нежели при плацебо, что подтвердило проаритмический потенциал натрий-канал-блокирирующих субстанций.
Но также антиаритмики, действующие через блокаду реполяризирующе действующих калиевых каналов (класс III), несут риск вентрикулярной проаритмии. При этих группах субстанций на передний план выходят из-за удлинение репорляризации вызываемые ранние последеполяризации и Torsade-de-Pointes тахикардии (TdP).
SWORD-исследование (Survival With Oral d-Sotalol) было прекращено, так как под действием d-Sotalol (чистый класса III антиаритмик без дополнительного бета-блокирующего действия) у пациентов с инфарктом сердца произошло больше случаев новых аритмий и смерти, чем под плацебо. Даже антиаритмическая терапия амиодароном у постинфарктных пациентов не приносит пользы по сравнению с плацебо в отношении общей смертности и кардиальной смертности.
С некоторого времени описываются и нежелательные кардиоваскулярные действия при определенных обстоятельствах также не-антиаритмически действующих субстанций, что частично привело к отзыву с рынка изготовителем самостоятельно или по распоряжению правительства. В дальнейшем мы более подробно коснемся этих неблагоприятных побочных эффектов некардиальных субстанций.
QT- интервал
Для реполяризации желудочка необходимое время может быть на ЭКГ измерено как QT- интервал. Удлиненная реполяризация распознается по удлинению QT-интервала.
Удлинение QT- интервала, с одной стороны, может оказывать антиаритмический эффект, а с другой стороны, благоприятствовать наступлению ранних после-реполяризаций и ассоциирует с возникновением TdP-тахикардий, которые или прекращаются спонтанно, или могут приводить к внезапной сердечной смерти. Явно удлинение QT-времени (или на частоту скорригированного QT-времени (QRc), является одним из основных признаков TdP-тахикардий.
QT- интервалы от 350 до 440 ms (мужчины <430 ms, женщины <450 ms) являются нормальными, потенциально вызывающими озабоченность считаются значения от 450 до 500 ms, повышенный риск аритмий возникает со значений 500 ms.
Наряду с врожденными формами удлинения QT (с глухотой или без глухоты) важную клиническую роль играют приобретенные формы. Наряду с удлинением QT описывают дополнительно увеличение QT-дисперсии, меру гетерогенности реполяризации.
Удлинение QT антиаритмиками
Удлинения QT и TdP тахикардии являются типичными побочными действиями различных антиаритмиков (табл. 1). Они отчасти возникают в зависимости от дозы и на ранней фазе терапии.
Преимущественно TdP тахикардии наблюдаются только после конверсии синусового ритма (во время относительной брадикардии), а не во время трепетания предсердий. Частота таких нарушений ритма составляет от 1% до 8% . Coplen провел метаанализ целого ряда рандомизированных исследований по хинидину по достижению синувого ритма после кардиоверсии трепетания предсердий. Терапия хинидином была сопряжена с более высокой смертностью (2,9% vs 0,8% контрольной группы).
Некоторые субстанции, например, амиодарон и Bepridil вызывают даже удлинения QT, но редко TdP. Амиодарон даже применяется у пациентов, у которых TdP развились в результате действия других препаратов. Это связано с тем, что амиодарон блокирует не только K+ каналы, но также и Na+ - и Са++ каналы, а также бетаадрено-рецепторы и снижает при этом риск ранних послереполяризаций и триг-гированных аритмий.
|
Таблица 1. QT -удлинение после антиаритмиков (mod . Nach Thomas et al .) |
|
|
Препарат |
Механизм действия |
|
Класс IA Chinidin, Disopyramid (Norpace, Rythmodul ), Procainamid* |
Na+-канал блокада Удлинение реполяризации |
|
Класс III N-Acetylprocainamid*, Amiodaron (Amiobeta , Amiodarex , Amiohexal , Cordarex , Tachydarin и др .), Bretylium*, Sotalol (Darob , Sotabeta , Sotagamma , Sotalex и д р.) |
К+-канал блокада |
|
Класс IV Bepridil*, Lidoflazin*, Prenylamin* |
Блокада кальциевых каналов |
|
* В Германии более не продаются |
|
На примере амиодарна можно также обратить внимание и на другую проблему. Речь идет о фармакокинетическом аспекте. Время полу-элиминации для амиодарона составляет 15-100 дней (в среднем 30 дней), для активных метаболитов дезэтиламиодарона в среднем 60 дней.
Так как Kumulations-steady-state устанавливается почти через 5 значений времени полувыделения, то легко представить себе что такие субстанции очень трудно контролируются. У 27 пациентов (55,4 + 2,4 года), получавшие в течение 1 года амиодарон, изначальные значения QTc составляли 453 + 7 ms. Между 9 и 12 месяцами они быстро достигли значений 479 + 9 ms. Мониторинг пациентов должен соответственно включать определения уровня в крови и анализ ЭКГ.
Комиссия по препаратам немецкого общества врачей уже довольно рано указывала на опасность удлинения QT антиаритмиками классов I и III. Также в отношении фиксированной комбинации Cordichin (160 mg Chinidin plus 80 mg Verapamil) указывалось на опасность развития TdP-тахиаритмий и трепетания желудочков.
Удлинение QT "не-кардиальными" препаратами
Наряду с классами IA и классом III антиаритмиков и некоторые другие фармакологические препараты, не считающиеся антиаритмиками или "сердечными средствами", также могут приводить к развитию удлинений QT и TdP-такхикардий.
Изъятия с рынка
За последние годы некоторые препараты в связи с тяжелыми нежелательными кардиоваскулярными эффектами были изъяты как с немецкого, так и с американского рынков.
Уже в начале 1998 года в США был отозван антигистаминный препарат Terfenadin (Teldane). В 1999 году последовал в Германии и США Astemizol, после того как появились первые указания на тяжелые нарушения ритма и остановку сердца - в основном у пациентов с тяжелыми нарушениями функции печени и/или при одновременном приеме ингибиторов энзимов.
Своим "Rote-Hand" письмом (27 октября 1999 г.) Glaxo Wellcome в Германии и США обратило внимание на изъятие Grepafloxacin, после того - хотя и очень редко - как он вызывал удлинения QT с риском развития тяжелых аритмий (TdP). Также нейролептик Sertindol был изъят с немецкого рынка из-за риска развития тяжелых нежелательных кардиоваскулярных проявлений (дозозависимое удлинение QT, внезапная сердечная смерть). В США Sertindol никогда не применялся.
В апреле 2000 года Janssen изъял с рынка прокинетик Cisaprid, после того как FDA зарегистрировала более 340 сообщений о нарушениях сердечного ритма из них 80 случаев закончившихся смертью. После чего и немецкие органы власти аннулировали разрешение цизаприд-содержащих препаратов из-за тяжелых побочных эффектов. По поводу этого Janssen-Cilag заявил протест.
Кроме того были описаны другие препараты удлиняющие QT (табл.2), имеющие самое разнообразное клиническое значение. Часто это касалось отдельных наблюдений, иногда пробандов или пациентов в клинических исследованиях.
|
Таблица 2. Удлинение QT после "не-кардиальных" препаратов |
|
|
Препарат |
Замечания |
|
Антипсихотики/нейролептики |
|
|
Chlorpromazin (Propaphenin)* |
Описание случая (100 mg/d) |
|
Haloperidol (Haldol и др.)* |
4 mg орально до >100 mg i.v. (описание случая) |
|
Primozid (Orap)* |
Здоровые пробанды (6 mg орально), |
|
Quetiapin (Seroquel)* |
Описание случая (комедикация с ингибитором CYP3A4 Lovastatin |
|
Thioridazin (Melleril)* |
Здоровые пробанды (59 mg орально), |
|
Антидепрессивные препараты |
|
|
Desipramin (Pertofran, Petylyl)* |
Описание случая (2,5 mg/kg/d) |
|
Doxepin (Aponal, Doneurin и др.)* |
Пациенты клиническом исследовании (169 mg/d) |
|
Nortriptylin (Nortrilen)* |
Описание случая (0,51 mg/kg/d) |
|
Amitriptylin (Amineurin, Saroten и др.) |
Пациенты клинического исследов. (150-200 mg/d) |
|
Fluoxetin (Fluctin, Fluxet и др.) |
Пациенты клин. Исследов. (37 mg/d) |
|
Maprotilin (Deprilept, Ludiomil и др.) |
Лписание случая (пациентка 69 лет, тяжелая сердечная недостаточность) |
|
Антигистаминные средства (2 поколение) |
|
|
Terfenadin (Histedin т др.)* |
Здоровые пробанды, пациенты с кардиоваскулярными заболеваниями (120-360 mg), |
|
Cetirizin (Alerid, Zyrtec) |
Здоровые пробанды (до 60 mg/d) |
|
Fexofenadin (Telfast) |
Здоровые пробанды, пациенты с аллергическим ренитом (180-240 mg/d), описание случая с попыткой реекспозиции |
|
Loratadin)Lisino) |
Здоровые пробанды (10 mg/d в комбинации с эритромицином), описание случая попытка суицида (300 mg) |
|
Mizolastin (Mizollen, zolium) |
Здоровые пробанды (40 mg/d) |
|
Антигистаминные (1 поколение) |
|
|
Chlorphenamin (Codicaps, Contac и др.) |
|
|
Diphenhydramin (Emesan и др.) |
|
|
Hydroxyzin (AN 3 N, Atarax и др.) |
|
|
Promethazin (Atosil, Prothazin и др.) |
|
|
Макролидные антибиотики |
|
|
Clarithromycin (Cylinid, Klacid и др.)* |
Описание случая (1000 mg/d орально) |
|
Пациенты (500-1000 mg i.v.) Описание случая (2000-4000 mg i.v.) |
|
|
Spiramycin (Rovamycine, Selectomycin)* |
Новорожденные (350 000 IE/kg/d орально |
|
Ингибиторы Gyrase |
|
|
Levoflaxin (Tavanic)* |
Описание случая (500 mg/d) |
|
Moxiflocxacin (Avalox)* |
Пациенты в клиническом исследовании (400 mg/d) |
|
Агонисты бета-2-адренорецепторов |
|
|
Fenoterol (Berotec, Partsisten)* |
|
|
Salbutamol (Apsomol, Sultanol и др.) |
Пациенты с мягкой астмой в клиническом исследовании |
|
Terbutalin (Bricanyl, Contimit, Terbul и др.) |
Пациенты с мягкой астмой в клиническом исследовании |
|
Противомалярийные |
|
|
Пациенты (1800 mg/d i.v.), здоровые пробанды, пациенты с гепатитом (10 mg/kg/i.v.) |
|
|
Halofantrin (Halfan)* |
Описание случая (1000 mg/d орально). Особенно у женщин следует избегать высоких доз. |
|
Препарат |
Замечания |
|
Прочие |
|
|
Пациенты в клиническом исследовании (фаза II), 0,15 mg/kg i.v./d max 60 дней |
|
|
Cyclophosphamid (Endoxan и др.)* |
5 из 19 пациентов при терапии в высоких дозах |
|
Ketoconazol (Nizoral, Terzolin)* |
Здоровые пробанды (400 mg/d орально) |
|
Pentamidin (Pentacarinat)* |
HIV-инфицированные пациенты (4 mg/kg/d) |
|
Tacrolimus (Prograf)* |
Описание случая (5 mg i.v. ежедн, 0,25 mg/час i.v.) |
|
Tiaprid (Tiapridex) |
Описание случая (300 mg/), 76 лет дополнительно легкая сердечная недостаточность. |
|
* Данные показались нам клинически особенно значимыми |
|
Антипсихотики
В одной из очень тщательно проведенных сравнительных работ было установлено, что у пациентов с шизофренией, получавших антипсихотическую медикацию (Chlorpromazin, Thioridazin, Levomepromazin и Haloperidol)в конвенциональной дозировке (n=59) по сравнению с пациентами не получавших антипсихотиков (n=5) и со здоровыми (n=45) удлинялись как значения QTc, так и QTc дисперсия. Вентрикулярные тахикардии однако в этом исследовании не отмечались, возможно из-за того, что отсутствовали другие факторы риска.
В одном из последних обзоров особенно часто отмечались ненормальные удлинения QTc (>456 ms) у пациентов старше 65 лет и получавших Droperidol или Thioridazin. Thioridazin и Mesoridazin (в Герма-нии не были в свободной продаже) были классифицированы FDA и ВОЗ как обладающие особенно повышенным риском.
Droperidol внутривенно в основном применялся при нейролептанальгезии. Janssen-Cilag стал его выпускать с 2001 года. Особенно подверженными оказались психиатрические неотложные пациенты, получавшие свои психотики парентерально и нередко дававшие гипокалиемию.
И наоборот, QTc удлинения вызываемые атипичными нейролептиками Risperidon, Quetiapin или Olanzapin оказались незначительными. Даже комедикация с ингибиторами энзимов, например, Ketoconarazol, Fluvoxamin или Paroxetin не оказывала негативного действия.
Антидепрессанты
Нежелательные кардиоваскулярные инциденты были описаны при различных трициклических антидепрессантах (Clomidin, Imipramin, Desipramin, Doxepin, Nortriptylin) не только при их передозировках, но в отдельных случаях и при применении обычных терапевтических доз. Сообщения о внезапной сердечной смерти были отмечены после Desipramin, Clomipramin и Imipramin.
У 69-летней пациентки с тяжелой сердечной недостаточностью при приеме Maprotilin (50 mg/d в течение нескольких лет) развились TdP тахикардия (QTc=700 ms). При этом определенно коморбидность сыграла решающую роль. Должны иметься четкие указания на значение коморбидности "кардиоваскулярного заболевания".
В отличие от этого оказывается, что после Fluoxetin и после Amitriptylin в рекомендованных дозировках не происходит удлинения QT. Также при применении Citalopram не описывалось до сих пор удлинения QT.
Антигистаминные препараты
В одном из случай-контролированных исследований были определены уровни частоты (95% интервал конфиденциальности) вентрикулярных аритмий на 10 000 персон/лет, например, для Astemizol 8,5 (2,8-26,5), для Cetrizin 3,6 (0,9-14,2), для Loratadin 1,5 (0,2-10,3) и для Terfenadin 1,0 (0,3-3,0). Женщины оказались несколько более подверженными, более чем мужчины, пациенты >50 лет явно поражались сильнее, чем более молодые.
Эта оценка риска преимущественно неседирующих Н1-антигистаминных препаратов 2-го поколения разделялась также другими авторами. Следует указать особенно на дозо-зависимость этих состояний, так как именно при самолечении антигистаминными препаратами опасность особенно велика, так как пациенты "титрируются" вплоть до полного исчезновения симптомов.
В кардиотоксичности Astemizol кажется основную роль играют два его главных метаболита Desmethylastemozol и Norastemizol.
За кардиальные инциденты, связанные с Terfenadin, в основном ответственна материнская субстанция. За это говорит и то, что кардиотоксичность усиливается ингибиторами энзимов, например, макролидными антибиотиками или антимикотиками. На здоровых мужчинах и женщинах можно продемонстрировать, что значения QTc могут позитивно коррелировать с уровнями в крови Terfenadin и Loratadin. Уровни в крови повышаются при дополнительном введении антидепрессивного препарата Nefazodon. Последний является ингибитором цитохром-Р-450-3А (CYP3A).
В настоящее время однако отсутствие кардиотоксичности Fexofenadin, метаболита Tefenadin, поставлено под вопросом. У 67-летнего мужчины QTc значение после экспозиции и реэкспозиции к Fexofenadin (180 mg/d) составляли 532 ms. - 512 ms. Базисные значения были однако немного удлинены (482-494 ms).
Кроме того, заслуживают внимания данные экспериментов на животных и отдельные клинические наблюдения того, что даже классические седирующие антигистаминика, и, прежде всего, Diphenhydramin и в высоких дозировках даже Hydrozysin могут индуцировать удлинение QT и ненормальную реполяризацию желудочков. Аритмогенные особенности описываются также и у Promethazin, Pheniramin и Chlorphenamin. Возможно, что при повышенном внимании такие инциденты могли бы чаще выявляться и классифицироваться.
Макролидные антибиотики
Между 1970 и 1996 годами FDA было зарегистрировано 346 наблюдений сердечных аритмий, связанных с эритромицином (58% женщин, 32% мужчин, 10% данные отсутствовали). У 49 пациентов речь шла о жизнеугрожающих аритмиях (вентрикулярные тахикардии, TdP, трепетания желудочков) и случаях смерти (33). Факторами риска были прежде всего высокие дозировки и внутривенное введение.
Эритромицин удлинял в зависимости от дозы длительность потенциала действия и снижал максимальный подъем потенциала действия в волокнах Purkinje. Эти электрофизиологические эффекты очень схожи с таковыми Chinididn.
В отношении Claritromycin уже в 1998 году имелось два инцидента с удлинением QT и TdP. На здоровых пробандах удлинение QT имело значение только в комбинации с прокинетикумом Cisaprid.
В эксперименте на животных на крысах было показано, что Roxithromycin и Azithromycin явно реже могли провоцировать аритмии, чем эритромицин или кларитромицин. По этой причине Roxithromycin в терапии должно отдаваться предпочтение.
Gyrase-ингибиторы
Из новых флюорхинолонов Grepafloxacin Glaxo Wellcome в связи с развитием TdP был изъят с рынка. Также в отношении Sparfloxacin и Moxifloxacin имелись соответствующие сообщения. Zagam в "Roten Liste 2002" более не указывался.
Также и в отношении Moxifloxacin (Avalox) изготовитель со всей очевидностью указывает на ограничения применения и противопоказания; не должны превышаться дозы 400 mg/d. Комедикация с другими проаритмическими препаратами не должна иметь места. Не советуется применение у пациентов с электролитными нарушениями и/или брадикардией.
Имеются отдельные описания нарушений ритма сердца при применении Ofloxacin, Levofloxacin и Enoxacin. Разрешение на применение Clinafloxicin из-за выраженных побочных действий, среди прочего на удлинение QT, было отозвано самими производителями Gödecke (или Parke-Davis).
Агонисты бета-2-адренорецептора
Об эпидемии смерти случаев от астмы в Японии сообщалось в 60-е годы 20 столетия в связи с Isoprenalin forte. 10 лет спустя тот же самый феномен был отмечен в связи с Fenoterol (200 mg на один выброс аэрозоля) в Новое Зеландии, в Sasktchewan (Kanada) и в Японии. Механизмы этой ассоциации известны недостаточно. Кардиоваскулярные эффекты однако исключать нельзя.
На 8 пациентах с астмой двойным слепым методом в Cross-over-исследовании было проведено сравнение действия Fenoterol, Salbutamol и Terbutalin с плацебо. Было выявлено выраженное дозо-зависимое удлинение значений QT при применении Fenoterola. Несколько меньшее, но явное, было удлинение QTc при применении наивысших доз Salbutamol и Terbutalin. Почти в тех же пропорциях происходило снижение содержания калия в плазме.
При сдержанном применении ингаляционных бета-агонистов такие проблемы в дальнейшем могли бы быть разрешены. Отношение чиновников здравоохранения к этому феномену в разных странах различно. В США Fenoterol не разрешен.
Halofantin
21 здоровый пробанд получали ежедневно 500 mg Halofantin в течение 42 дней и находились под наблюдением в течение последующих 138 дней. Среднее время полураспада составляло 7 + 5 дней. Удалось продемонстрировать явную зависимость от концентрации удлинения интервалов QTc.
Cyclophosphamid, Ketoconazol
Высокие дозы (1400 mg/m2 в течение 4 дней) Cyclophosphamid вызывали у некоторых пациентов удлинение значений QT-дисперсии (43,2-83,2 ms); при этом затем возникала острая недостаточность левого сердца. Возможно эти инциденты в основном возникают тогда, когда имеют значения дополнительные обусловленные антрациклином поражения сердца.
Также Ketoconazol (200 mg 12 часов в течение 5 дней), антимикотик, вызывал у здоровых пробандов небольшие, но существенные удлинения значений QTc.
Vasodilatatoren
Также ранее применявшиеся как вазодилататоры, теперь исключенные из продажи в Германии субстанции такие, как Lidoflazin, Prenylamin, Bepridil обладают дозо-зависимым присущим классу-1А-эффектом, который имел особое клиническое значение для пожилых пациентов и мог вызывать TdP-тахикардии.
Антагонисты серотонина
Также во время лечения антагонистами серотонина Ketanserin и Zimedin были описаны явные удлинения времени QT и TdP-тахикардии; и почти всегда при наличии дополнительных благоприятствующих факторов (гипокалиемия, брадикардия). Обе субстанции в Германии не продаются. От Zimedin во всем мире отказались еще в 1983 году.
Факторы риска удлинения QT и TdP
Зависимость от пола
Обычно женщины находятся под более высоким риском удлинения QT и TdP, чем мужчины (табл.3).
|
Таблица 3 |
|
|
Зависимость от пола У женщин имеется больший риск изменений QT и возникновения Torsades-de-Pointes явно зависящий от менструального цикла |
|
|
Врожденные формы* Romano-Ward-Syndrome Jervell-Lange-Nielsen-Syndrome (с глухотой внутреннего уха) |
|
|
Приобретенные формы |
|
|
Электролитные нарушения |
Гипокалиемия, гипомагнезиемия, гипокальциемия |
|
Нарушения обмена веществ |
Гипотиреоз, гиперпаратиреоидизм, гиперальдостеронизм, феохромоцитома, диабет (автономная нейропатия) |
|
Нарушения ЦНС |
Интракраниальные, субарахноидальные кровоивзлияния, острый синус-тромбоз, энцефалит, ранения головы |
|
Кардиальные нарушения |
Миокардит, опухоль сердца, высокой степени AV-блокада, дисфункция синусовых узлов, клинически значимая брадикардия (<50 el|vby/) |
|
Нарушения питания |
Голодание, диета "жидким протеином" |
|
* Болезни ионных каналов с кардиальными аритмиями |
|
Из 346 эритромицин-обусловленных аритмий 58% приходилось на женщин и 32% на мужчин (в 10% данные отсутствовали). Этот эффект был подтвержден на изолированных сердцах кроликов при перфузии эритромицином.
В настоящее время этот эффект был описан снова в отношении Chinidin. Среди участвующих пробандов в любом случае женщины имели уже более высокие исходные значения QTc (407 = 7 ms), чем мужчины (395 + 9 ms), вызванные Chinidin удлинения составили 42 + 3 ms до 29 + 3 ms.
С помощью экспериментально индуцированных (антиаритмик Ibutilid 0,003 mg/kg i.v. 10 мин.) QT-удлинений у женщин удалось показать, что наибольшие изменения определялись во время первой половины менструального цикла (созревание фолликулов/фаза пролиферации).
Внезапная смерть в детском возрасте
Имеются указания на то, что удлинение QT-интервала у новорожденных на 1 неделе жизни явно ассоциировало с "sudden infant death syndrome". Рутинный ЭКГ-скрининг новорожденных, однако, пока еще не рекомендован.
Электролитные изменения
Нарушения электролитов, медикаментозно ли индуцированных (например,диуретиками), или в виде сопутствующих заболеваний, такими как нарушения обмена веществ, заболевания ЦНС, сердца и нарушения питания могут благоприятствовать возникновению TdP тахикардий. Недавно у 12-летней девочки было описано удлинение QTc вследствие вызванной псевдогипопаратиреодизмом гипокаль-циемии.
Следует напомнить, что гипокалиемии могут вызываться диуретиками (Thiazid, Furosemid), Amphotericin B i.v., кортикостероидами и злоупотреблением Laxanzien. Гипомагнезиумемии известные как "soft-water-factor". Причины могут быть разнообразны, например, географические области с "мягкой водой", бедные фосфатами растительные продукты, современные способы приготовления пищи, фосфат-содержащие напитки такие как кола, чрезмерное потоотделение (спорт, сауна), заболевания и многие медикаменты.
Брадикардии
Брадикардии, благоприятствующие наступлению ранних последеполяризаций, могут среди прочего вызываться сердечными гликозидами или бета-рецепторблокаторами. Также при брадикардиях усиленных антиаритмиками (синусовые брадикардии или AV-блокады) и после аблации пучка Гиса у пациентов с до вмешательства с тахикардно сверхпроводимым трепетанием предсердий, описываются TdPтахикардии.
Передозировка лекарственных препаратов
Так как токсические побочные действия возникают в зависимости от дозы, то передозировки медикаментов всегда связаны с особым риском. Причины тому многообразны: абсолютно небрежная ошибочная передозировка врачом или пациентом, передозировка лекарственных препаратов в результате недоучета при установлении дозы ограниченной функции почек, печени и/или щитовидной железы. В пожилом возрасте особую роль играет часто уменьшенный объем распределения.
Может иметь значение и то, что для многих субстанций существуют медленные и быстрые метаболизаторы. Медленные метаболизаторы наиболее подвержены риску. В отношении Цитохром-Р-450 изоэнзим среди лиц кавказской расы имеется 5-8% медленных выделителей.
Взаимодействия лекарственных препаратов
В начале 90-х стало очевидным, что терфенадин-содержащие препараты противопоказаны не только пациентам с тяжелыми нарушениями функции печени, но также и одновременный прием других препаратов, например, Ketoconazol или макролидных антибиотиков эритромицина, Josamycin, Troleandomycin, что может быть связано с высоким риском жизнеугрожающих вентрикулярных нарушений ритма. В дальнейшем снова описывались соответствующие открытия, например, QTc-удлинение у здоровых пробандов при комбинации Cisaprid с Clarithromycin было значительно интенсивней, чем при применении каждой субстанции в отдельности.
К ингибиторам энзимов относятся различные макролидные антибиотики, прежде всего Erythromycin, Clarithromicin и Troleandomycin (и наоборот, не Rqxithromycin, Rulid), Chloramphenicol, Ciprofloxacin, Azol-Antmycotica, например Fluvoxamin, Fluoxetin, HIV-ингибиторы протеаз, например, Indinavir, Nelfinavir, Ritonavir, Saquinavir, Н2-рецептор-анатгонисты (но не Famotidin), а также HMG-CoA-редуктазы ингибитор Lovastatin, который ингибирует изоэнзим CYP3A4; здесь Pravastatin мог бы явиться альтернативой.
Все больший интерес вызывает тот факт, что сок грейфрута подавляет метаболизм многих субстанций, метаболизируемых с помощью CYP3A4, например Dihydropyridin-кальций антогонистов, Cyc-losporin, Midazolam, Triazolam, Terfenadin и Amiodaron. Также при этом могут развиться осложнения.
Заключение
Если у пациентов развиваются TdP во время проводимого лечения, то должны быть отменены все подозрительные препараты и скоррегированы все электролитные нарушения. Если отсутсвтуют альтернативные медикаменты, но необходимо провести очень тщательный индивидуальный подбор дозы, с учетом коморбидности и комедикации пациентов. Сообщение о соответствующем инциденте должно быть направлено в фармакологическую комиссию немецкого общества врачей или в фармацевтическую индустрию.
Введение
Наследственный синдром удлинённого интервала QT (СУИQT, в англоязычной литературе - Long QT syndrome - LQTS или LQT) является наиболее частым и наиболее изученным из данных заболеваний, проявляющимся удлинением интервала QT на ЭКГ [при отсутствии других вызывающих это изменение причин], рецидивирующими синкопальными и пресинкопальными состояниями вследствие пароксизмов TdP, а также случаями внезапной сердечно-сосудистой смерти.Эпидемиология
Распространенность заболевания в популяции составляет около 1:2000 новорождённых. Следует отметить, что эти данные учитывают только случаи «явного» увеличения продолжительности интервала QT, выявленного при регистрации ЭКГ. У некоторых больных симптомы заболевания могут полностью отсутствовать в течение всей жизни и проявляться лишь при возникновении дополнительных факторов , способствующих удлинению интервала QT, например гипокалемии , или при назначении лекарственных препаратов, способных увеличивать длительность интервала QT. Кроме того, удлинение интервала QT может носить преходящий характер, следовательно, истинная распространённость данного заболевания в популяции, по-видимому, ещё больше.Этиология
Основной причиной СУИQT является дисфункция ионных каналов и насосов, приводящая к увеличению продолжительности фаз реполяризации кардиомиоцитов. Нарушение функции ионных каналов может быть обусловлено мутацией в генах основных порообразующих α-субъединиц, добавочных субъединиц, осуществляющих регуляцию их функции, белков-переносчиков, необходимых для транспортировки молекул, а также вспомогательных белков, опосредующих «встраивание» молекул в биологические мембраны и взаимодействие с клеточными структурами.Классификация и клинические проявления
В табл. 1 представлена генетическая классификация синдрома удлиненного интервала QT: указаны гены, мутации в которых обнаруживают при соответствующих типах заболевания, кодируемые данными генами белки и изменения ионных токов, приводящие к удлинению фаз реполяризации. Следует отметить, что при проведении молекулярно-генетического скрининга больных СУИQT примерно в 25% случаев генетические нарушения не обнаруживают, что позволяет ожидать в дальнейшем выявление новых генетических мутаций, приводящих к возникновению заболевания.Таблица 1. Молекулярно-генетические типы наследственного синдрома удлинённого интервала QT
Описаны следующие фенотипические формы синдрома удлиненного интервала QT: синдром Романо–Уорда (Romano–Ward), синдром Джервелла и Ланге–Нильсена (Jervell and Lange-Nielsen), синдром Андерсена–Тавила (Andresen–Tawil) и синдром Тимоти (Timothy).
Наиболее распространённая форма заболевания с аутосомно-доминантным типом наследования - синдром Романо–Уорда (Romano–Ward), характерными клиническими проявлениями которого являются увеличение продолжительности интервала QT, рецидивирующие синкопальные состояния, чаще всего обусловленные полиморфной желудочковой тахикардией (ЖТ) типа пируэт, и наследственный характер заболевания. Более 90% случаев синдрома Романо–Уорда представлены СУИQT 1-го (СУИQT1), 2-го (СУИQT2) и 3-го (СУИQT3) типов, имеющих особенности клинических и электрокардиографических проявлений (табл. 2, рис. 1).
Таблица 2. Клиническая характеристика основных типов наследственного синдрома удлинённого интервала QT.

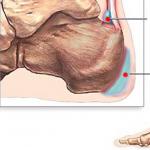
 Рис. 1.
Изменения ЭКГ при различных типах наследственного синдрома удлиненного интервала QT: (А) - широкая гладкая волна T при СУИQT1; (Б) - двухфазная T-волна при СУИQT2; (В) - низкоамплитудная и укороченная T-волна с удлиненным, горизонтальным ST-сегментом при СУИQT3.
Рис. 1.
Изменения ЭКГ при различных типах наследственного синдрома удлиненного интервала QT: (А) - широкая гладкая волна T при СУИQT1; (Б) - двухфазная T-волна при СУИQT2; (В) - низкоамплитудная и укороченная T-волна с удлиненным, горизонтальным ST-сегментом при СУИQT3.
СУИQT1 - наиболее распространенный тип синдрома, обусловленный мутацией в гене KCNQ1, кодирующем α-субъединицу калиевого канала, генерирующего ток IKs, который является основным током реполяризации при высокой частоте сердечного ритма. Снижение силы IKs приводит к недостаточному укорочению интервала QT при нарастании частоты сердечных сокращений. По этим причинам больным СУИQT1 характерно возникновение TdP на фоне физической нагрузки (рис. 2) и эмоционального стресса. Особенностью ЭКГ при СУИQT1 является удлиненная и гладкая волна Т (см. рис. 1А).

Рис. 2. Развитие пароксизма полиморфной желудочковой тахикардии типа Torsade de Pointes на фоне физической нагрузки у больной синдромом Романо–Уорда (фрагмент непрерывной записи суточного мониторирования ЭКГ по Холтеру).
Причиной СУИQT2 является мутация в гене KCNH2, кодирующем α-субъединицу калиевого канала Kv11.1, генерирующего ток IKr. При СУИQT2 пароксизмы TdP могут возникать как во время нагрузки, так и в покое. Характерным провоцирующим фактором является резкий громкий звук. На ЭКГ больных СУИQT2 регистрируют непротяженную, двухфазную волну Т (см. рис. 1Б).
СУИQT3 является менее распространённой формой заболевания, обусловленной мутацией в гене SCN5A, кодирующем α-субъединицу натриевого канала, что приводит к нарушению инактивации натриевых каналов, продолжающемуся вхождению ионов Na+ в клетку и увеличению продолжительности реполяризации кардиомиоцитов. TdP у больных СУИQT3 возникают на фоне брадикардии , преимущественно во время сна. Физические нагрузки, напротив, переносятся хорошо и сопровождаются укорочением интервала QT. Характерной особенностью ЭКГ у данных больных является удлиненный сегмент ST с отсроченным началом непродолжительной низкоамплитудной волны Т (см. рис. 1В).
Существенно реже встречается аутосомно-рецессивная форма заболевания (синдром Джервелла и Ланге–Нильсена), для которой характерны врождённая нейросенсорная тугоухость, более выраженное увеличение длительности интервала QT и большая частота опасных для жизни желудочковых аритмий. Заболевание обусловлено мутациями в генах KCNQ1 или KCNE2, кодирующих основную и добавочную субъединицы потенциал-зависимых калиевых каналов Kv7.1, приводящими к снижению силы тока IKs.
Синдром Андерсена–Тавила - редкая форма заболевания, при которой удлинение интервала QT сопровождается появлением волны U, пароксизмами как полиморфной желудочковой тахикардии типа TdP, так и двунаправленной желудочковой тахикардии. В 60% случаев заболевание обусловлено мутацией в гене KCNJ2, кодирующем α-субъединицу калиевых каналов аномального входящего выпрямления Kir2.1, генерирующих ток IK1, сила которого снижается. В 40% случаев генетический дефект в настоящее время обнаружить не удаётся. Характерные экстракардиальные проявления заболевания, такие как, аномалии развития костной системы (низкорослость, микрогнатия, большое расстояние между глазницами, низкое расположение ушных раковин, сколиоз, клинодактилиия), гипокалемия и периодический калий-зависимый паралич, присутствуют не у всех больных. Синдром Андерсена–Тавила - заболевание с аутосомно-доминантным типом наследования, однако семейный характер заболевания прослеживается далеко не всегда, в связи с трудностями диагностики, неспецифическими клиническими проявлениями заболевания и неполной пенетрантностью мутантных генов. До 50% случаев заболевания обусловлены мутацией de novo
Синдром Тимоти - крайне редкая форма СУИQT, обусловленная мутацией в гене CACNA1c, кодирующем α-субъединицу кальциевых каналов CaV1.2. При данном синдроме отмечают наиболее выраженное удлинение интервалов QT и QTc (до 700 мс), сопровождающееся крайне высоким риском внезапной сердечно-сосудистой смерти (средняя продолжительность жизни составляет 2,5 года). До 60% больных имеет различные врождённые пороки сердца [открытый артериальный проток, тетраду Фалло , открытое овальное окно и дефекты межжелудочковой перегородки] и различные нарушения проводимости (характерны преходящая и постоянная формы АВ блокады II степени с проведением на желудочки 2:1). Среди экстракардиальных проявлений заболевания описаны когнитивные нарушения (задержка психомоторного развития, аутизм), гипогликемия , иммунодефициты, аномалии строения лица (сглаженность носогубной складки, низкое расположение ушных раковин), а также частичное или полное сращение пальцев кистей и стоп (синдактилия). Синдром Тимоти наследуется по аутосомно-доминантному типу, однако подавляющее большинство случаев заболевания обусловлено мутацией de novo.
Диагностика
Критерии, применяемые для постановки диагноза наследственного СУИQT, предложенные J.P. Schwarz, представлены в табл. 3. Таблица 3. Диагностические критерии наследственного синдрома удлинённого интервала QT (в соответствии с изменениями 2006г.).
Наследственный СУИQT диагностируют в случае, если сумма баллов составляет ≥3,5, при наличии подтверждённой молекулярно-генетическими методами мутации, приводящей к увеличению продолжительности интервала QT, при повторной регистрации на ЭКГ удлинения интервала QTc ≥600 мс в случае отсутствия других причин удлинения интервала QT.
Диагноз наследственного СУИQT может быть также поставлен при повторной регистрации на ЭКГ удлинения интервала QTc до 480–499 мс у пациентов с синкопальными состояниями неясного генеза, при отсутствии генетической мутации и других причин удлинения интервала QT.
Методы молекулярно-генетической диагностики имеют большое значение в диагностике СУИQT и определении прогноза больных. При проведении комплексных генетических анализов мутации удаётся обнаружить приблизительно у 75% больных, поэтому отрицательный результат генетического анализа не позволяет полностью исключить диагноз СУИQT.
Проведение комплексного генетического анализа на выявление возможных мутаций в генах KCNQ1 KCNH2 и SCN5A (СУИQT 1, 2 и 3-го типов - наиболее распространённые формы заболевания) рекомендовано всем больным, имеющим клинические проявления СУИQT, отягощённый семейный анамнез и удлинение интервала QTc, зарегистрированное на ЭКГ в покое или при проведении провокационных диагностических проб, а также всем пациентам, не имеющим характерных СУИQT симптомов, при регистрации на ЭКГ удлинения интервала QTc >500 мс при отсутствии других возможных причин удлинения интервала QT.
Проведение комплексного генетического анализа на выявление возможных мутаций в генах KCNQ1 KCNH2 и SCN5A может иметь смысл у пациентов, не имеющих характерных СУИQT симптомов, при регистрации на ЭКГ удлинения интервала QTc >480 мс при отсутствии других возможных причин удлинения интервала QT.
В случае обнаружения у больного СУИQT генетической мутации проведение скрининга, направленного на выявление этой мутации, рекомендовано всем близким родственникам, даже при отсутствии у них характерных этому заболеванию клинических проявлений и изменений ЭКГ.
Поскольку удлинение интервала QT может носить преходящий характер, в диагностике заболевания имеют значение продолжительная регистрация ЭКГ (например, суточное мониторирование ЭКГ по Холтеру; данный метод особенно информативен у больных СУИQT 2-го и 3-го типов, поскольку у больных этими формами заболевания наибольшее увеличение длительности интервала QT отмечают обычно в ночное время) и провокационные пробы.
В целях обеспечения безопасности пациента и повышения диагностической значимости, существует ряд требований, которые должны быть учтены при проведении данных диагностических исследований. Поскольку в ходе исследований возможна индукция опасных для жизни нарушений ритма сердца, все провокационные пробы должны проводиться опытным медицинским персоналом при непрерывной регистрации ЭКГ (следует производить мониторирование ЭКГ до полной нормализации индуцированных в ходе исследования изменений ЭКГ, при проведении фармакологических провокационных проб - не менее 30 мин после окончания введения препарата) и систематическом измерении АД больного, в условиях непосредственной доступности необходимого для сердечно-легочной реанимации оборудования [включая дефибриллятор] и возможности незамедлительного вызова врача-реаниматолога. Проведение нагрузочных проб должны осуществлять физически тренированные сотрудники, способные уберечь пациента от падения в случае возникновения гемодинамического коллапса при индукции желудочковых аритмий.
Провокационные пробы далеко не всегда вызывают типичные для конкретного заболевания изменения ЭКГ. Пограничные изменения не должны расцениваться как диагностически значимые. В случае пограничных изменений ЭКГ или отрицательного результата исследования при большой вероятности заболевания (характерная клиническая картина, результаты генетических исследований) целесообразно проведение другой провокационной пробы.
Для выявления СУИQT используют следующие провокационные пробы.
- Активная ортостатическая проба. Оценка динамики интервала QT при регистрации ЭКГ в ходе ортостатической пробы обладает диагностической значимостью, позволяя в ряде случаев выявить больных СУИQT. После перехода в вертикальное положение отмечается умеренное увеличение частоты синусового ритма , при этом у здоровых пациентов длительность интервала QT уменьшается, а у больных СУИQT (особенно 2-го типа) продолжительность интервала QT уменьшается менее существенно, не изменяется или увеличивается.
- Проба с дозированной физической нагрузкой на велоэргометре или тредмиле. Наиболее информативна оценка длительности интервала QT в период восстановления. Длительность интервала QTc >445 мс в конце периода восстановления (спустя 4 минуты после окончания нагрузки) характерна для больных СУИQT 1-го и 2-го типов. При этом длительность интервала QTc <460 мс в начале периода восстановления позволяет отличить больных СУИQT 2-го типа от больных СУИQT 1-го типа.
- Проба с адреналином (эпинефрином). Позволяет выявить больных СУИQT1, поскольку при этой форме заболевания при проведении инфузии адреналина отмечается парадоксальное увеличение длительности интервала QT. Предложены 2 протокола проведения данной пробы: протокол Шимицу (Schimizu), в ходе которого вслед за болюсным введением осуществляется кратковременная инфузия адреналина, и протокол Мейо (Mayo), в соответствии с которым осуществляется внутривенная инфузия постепенно увеличиваемой дозы адреналина. Оба этих протокола обладают сопоставимыми чувствительностью и специфичностью, хорошо переносятся и редко сопровождаются нежелательными реакциями. Проба расценивается как положительная при увеличении длительности интервала QT >30 мс на фоне инфузии адреналина в дозе до 0,1 мкг/кг в мин. Следует отметить, что правильное измерение длительности QT на фоне инфузии адреналина часто затруднено изменениями морфологии зубцов T, особенно если при этом регистрируются высокоамплитудные волны U. Сопутствующий прием β-адреноблокаторов снижает диагностическую значимость пробы. Среди нежелательных реакций, возникающих на фоне инфузии адреналина, необходимо упомянуть артериальную гипертензию и индукцию опасных для жизни нарушений ритма. Диагностическое исследование должно быть прекращено при повышении систолического АД >200 мм рт.ст. (или при меньших значениях в случаях, если артериальная гипертензия сопровождается выраженными клиническими проявлениями), возникновении рецидивирующих неустойчивых пробежек или индукции устойчивого пароксизма ЖТ. В случае возникновения клинически значимых нежелательных эффектов целесообразно применение короткодействующих β-адреноблокааторов, вводимых внутривенно.
- Проба с аденозином. Больным СУИQT характерно увеличение продолжительности интервалов QT >410 мс и QTc >490 мс, регистрируемые во время минимальной частоты сердечных сокращений при индуцированной аденозином брадикардии. В настоящее время диагностическая значимость данной пробы изучена на ограниченном количестве больных генетически подтвержденным СУИQT, поэтому интерпретация полученных в ходе исследования результатов требует осторожности.
Дифференциальная диагностика
СУИQT следует дифференцировать от других возможных причин синкопальных состояний, учитывая относительно молодой возраст больных, прежде всего, от эпилепсии и вазо-вагальных обмороков, а также от других врождённых желудочковых нарушений ритма сердца. Необходимо проведение дифференциальной диагностики между врождённой и приобретёнными формами СУИQT, которые могут быть вызваны целым рядом факторов, приводящих к замедлению процессов реполяризации миокарда желудочков. К ним относятся:- брадикардия, обусловленная дисфункцией синусового узла или АВ блокадой;
- приём лекарственных препаратов (перечень препаратов, удлиняющих интервал QT).
Частота негативных кардиоваскулярных эффектов психотропной терапии, по данным масштабных клинических исследований, достигает 75%. Психически больные имеют достоверно более высокий риск внезапной смерти. Так, в сравнительном исследовании (Herxheimer A. et Healy D., 2002) показано 2-5-кратное увеличение частоты внезапной смерти у пациентов с шизофренией в сравнении с двумя другими группами (больные глаукомой и псориазом). Американское агентство по контролю за продуктами питания и лекарствами (USFDA) сообщило об 1,6-1,7- кратном повышении риска внезапной смерти при использовании всех современных антипсихотических препаратов (как классических, так и атипичных). Одним из предикторов внезапной смерти при терапии психотропными препаратами считают синдром удлинённого интервала QT (CУИ QT).
Интервал QT отражает электрическую систолу желудочков (время в секундах от начала комплекса QRS до конца зубца Т). Его продолжительность зависит от пола (у женщин QT длиннее), возраста (с возрастом QT удлиняется) и частоты сердечных сокращений (чcc) (обратно пропорционально). Для объективной оценки интервала QT в настоящее время пользуются корригированным (с поправкой на чсс) интервалом QT (QTc), определяемым по формулам Базетта и Фредерика:
В норме QTc составляет 340-450 мсек для женщин и 340-430 мсек для мужчин.
Известно, что СУИ QT опасен развитием фатальных желудочковых аритмий и фибрилляции желудочков. Риск внезапной смерти при врожденном СУИ QT в отсутствие адекватного лечения достигает 85%, при этом 20% детей умирают в течение года после первой потери сознания и более половины – в первое десятилетие жизни.
В этиопатогенезе заболевания ведущая роль отводится мутациям в генах, кодирующих калиевые и натриевые каналы сердца. В настоящее время идентифицировано 8 генов, ответственных за развитие клинических проявлений СУИ QT. Кроме того доказано, что у больных СУИ QT имеется врожденный симпатический дисбаланс (асимметрия иннервации сердца) с преобладанием левосторонней симпатической иннервации.
Гены, ответственные за развитие СУИ QT
В клинической картине заболевания доминируют приступы потери сознания (синкопе), связь которых с эмоциональным (гнев, страх, резкие звуковые раздражители) и физическим стрессом (физическая нагрузка, плавание, бег) подчеркивает важную роль симпатической нервной системы в патогенезе СУИ QT.
Продолжительность потери сознания составляет в среднем 1-2 минуты и в половине случаев сопровождается эпилептиформными, тонико-клоническими судорогами с непроизвольным мочеиспусканием и дефекацией. Поскольку синкопальные состояния могут встречаться и при других заболеваниях, часто таких пациентов трактуют как больных с эпилепсией, истерией.
Особенности синкопальных состояний при СУИ QT:
Как правило, возникают на высоте психоэмоциональной или физической нагрузки
типичны предвестники (внезапная общая слабость, потемнение в глазах, сердцебиение, тяжесть за грудиной)
быстрое, без амнезии и сонливости, восстановление сознания
отсутствие изменений личности, характерных для больных эпилепсией
Синкопальные состояния при СУИ QT обусловлены развитием полиморфной желудочковой тахикардии типа «пируэт» («torsades de pointes») (TdP). TdP называют ещё «сердечным балетом», «хаотической тахикардией», «желудочковой анархией», «сердечным штормом», что по сути является синонимом остановки кровообращения. TdP – неустойчивая тахикардия (общее количество QRS комплексов при каждом приступе колеблется от 6 до 25-100), склонная к рецидивам (уже через несколько секунд или минут приступ может повториться) и переходу в фибрилляцию желудочков (относится к жизнеугрожающим аритмиям). К другим электрофизиологическим механизмам внезапной кардиогенной смерти пациентов с СУИ QT относят электромеханическую диссоциацию и асистолию.
ЭКГ-признаки СУИ QT.
1 Удлинение интервала QT- превышающее норму для данной чсс более чем на 50мс, независимо от причин, лежащих в его основе, общепризнанно считается неблагоприятным критерием электрической нестабильности миокарда.
Комитет по патентованным лекарственным средствам Европейского Агентства по оценке медицинских продуктов (European Agency for the Evaluation of Medical Products) предлагает следующую интерпретацию продолжительности интервала QTc
Увеличение QTc на 30-60мс у пациента, принимающего новые лекарственные средства, должно вызывать настороженность в отношении возможной связи с препаратом. Абсолютную продолжительность QTc свыше 500мс и относительное увеличение более чем на 60мс следует рассматривать в качестве угрозы TdP.
2. Альтернация зубца Т – изменение формы, полярности, амплитуды зубца Т свидетельствует об электрической нестабильности миокарда.
3. Дисперсия интервала QT – разница между максимальным и минимальным значением интервала QT в 12 стандартных отведениях ЭКГ. QTd = QTmax – QTmin, в норме QTd = 20-50мс. Увеличение дисперсии интервала QT свидетельствует о готовности миокарда к аритмогенезу.
Отмечаемый в последние 10-15 лет растущий интерес к исследованию приобретенного СУИ QT расширил наши представления о внешних факторах, таких как различные заболевания, метаболические нарушения, электролитный дисбаланс, лекарственная агрессия, вызывающих нарушения функционирования ионных каналов сердца, аналогичные врожденным мутациям при идиопатическом СУИ QТ.
Клинические состояния и заболевания, тесно ассоциированные с удлинением интервала QT
Согласно данным, приведенным в докладе Центров по контролю и предупреждению заболеваний (Centers for Disease Control and Prevention) от 2.03.2001г., в США растет частота внезапной сердечной смерти среди людей молодого возраста. Высказывается мнение, что среди возможных причин этого роста важную роль играют лекарственные средства. Объем потребления лекарств в экономически развитых странах постоянно увеличивается. Фармацевтика давно стала таким же бизнесом как и любой другой. Только на разработку нового продукта у фармацевтических гигантов в среднем уходит около 800 млн. долларов, что на два порядка выше, чем в большинстве других областей. Наметилась отчетливая негативная тенденция в проведении фармкомпаниями все большего числа препаратов как статусных или престижных (lifestyle drugs). Такие лекарства принимают не потому, что они нужны для лечения, а потому что они соответствуют определенному образу жизни. Это «Виагра» и ее конкуренты «Сиалис» и «Левитра»; «Ксеникал» (средство для похудения), антидепрессанты, пробиотики, антигрибковые и многие другие препараты.
Другую тревожную тенденцию можно обозначить как Disease Mongering (торговлю болезнями). Крупнейшие фармкомпании, чтобы расширить рынок сбыта, убеждают вполне здоровых людей в том, что они больны и нуждаются в медикаментозном лечении. Количество мнимых недугов, искусственно раздуваемых до масштабов серьезных заболеваний, постоянно увеличивается. Синдром хронической усталости (синдром менеджера), климакс как заболевание, женская половая дисфункция, иммунодефицитные состояния, йоддефицит, синдром беспокойных ног, дисбактериоз, «новые» инфекционные заболевания становятся брендами для наращивания продаж антидепрессантов, иммуномодуляторов, пробиотиков, гормонов.
Самостоятельный и бесконтрольный прием лекарственных средств, полифармация, неблагоприятные комбинации препаратов и необходимость длительного приема лекарственных средств создают предпосылки для развития СУИ QT. Таким образом, индуцированное лекарствами удлинение интервала QT как предиктор внезапной смерти, приобретает масштабы серьезной медицинской проблемы.
Разнообразные лекарственные препараты самых широких фармакологических групп способны приводить к удлинению интервала QT.
Лекарственные препараты, удлиняющие интервал QT
Список препаратов, удлиняющих интервал QT, постоянно пополняется.
Все лекарственные средства центрального действия удлиняют интервал QT, зачастую клинически значимо, и именно поэтому проблема лекарственно-индуцированного СУИ QT в психиатрии стоит наиболее остро.
В серии многочисленных публикаций доказана связь между назначением антипсихотиков (как старых, классических, так и новых, атипичных) и СУИ QT, TdP и внезапной смертью. В Европе и США предоставление лицензии для нескольких нейролептиков не допускали или откладывали, другие были сняты с производства. После сообщений о 13 случаях внезапной необъяснимой смерти, связанной с приёмом пимозида, в 1990 году было принято решение об ограничении его суточной дозы до 20 мг в сутки и лечении под контролем ЭКГ. В 1998 году после публикации данных о связи приёма сертиндола с 13 случаями серьёзной, но не фатальной аритмии (36 смертельных случаев были предположительными) Лундбек добровольно временно прекратил продажу препарата на 3 года. В том же году по поводу удлинения интервала QT тиоридазин, мезоридазин и дроперидол получили предостережение в форме «чёрной вставки», а зипразидон – полужирным шрифтом. К концу 2000 года после смерти 21 человека вследствие приёма назначенного врачами тиоридазина, этот препарат стал препаратом второй очереди в лечении шизофрении. Вскоре после этого дроперидол был отозван с рынка его производителями. В Соединённом Королевстве выпуск атипичного антипсихотического препарата зипразидона откладывают, поскольку более чем у 10% пациентов, принимающих этот препарат, возникло лёгкое удлинение интервала QT.
r />Из антидепрессантов кардиотоксический эффект в наибольшей степени проявляют циклические антидепрессанты. По данным исследования 153 случаев отравления ТЦА (из которых 75% приходилось на амитриптилин) клинически значимое удлинение интервала QTс отмечалось в 42% случаев.
Из 730 детей и подростков, получавших антидепрессанты в терапевтических дозах, удлинение интервала QTс > 440 ms сопровождало лечение дезипрамином в 30%, нортриптилином в 17%, имипрамином в 16%, амитриптилином в 11% и кломипрамином в 11%.
Описаны случаи внезапной смерти, тесно ассоциированной с СУИ QT , пациентов, длительно получавших трициклические антидепрессанты, в т.ч. с посмертной идентификацией “slow-metabolizer” фенотипа CYP2D6 вследствие кумуляции препарата.
Новые циклические и атипичные антидепрессанты более безопасны в отношении кардиоваскулярных осложнений, демонстрируя удлинение интервала QT и TdP лишь при превышении терапевтических доз.
Большинство психотропных препаратов, широко используемых в клинической практике, относятся к классу В (по W. Haverkamp 2001), т.е. на фоне их применения имеется относительно высокий риск возникновения TdP.
По данным экспериментов in vitro, in vivo, секционных и клинических исследований антиконвульсанты, антипсихотики, анксиолитики, нормотимики и антидепрессанты способны блокировать быстрые калиевые HERG-каналы, натриевые каналы (вследствие дефекта гена SCN5A) и кальциевые каналы L-типа, вызывая, таким образом, функциональную недостаточность всех каналов сердца.
Кроме того, в формировании СУИ QT принимают участие хорошо известные кардиоваскулярные побочные эффекты психотропных препаратов. Многие транквилизаторы, нейролептики, препараты лития, ТЦА снижают сократимость миокарда, что в редких случаях может привести к развитию застойной сердечной недостаточности. Циклические антидепрессанты способны накапливаться в сердечной мышце, где их концентрация в 100 раз превышает уровень в плазме крови. Многие психотропные препараты являются ингибиторами кальмодулина, что приводит к нарушению регуляции синтеза протеинов миокарда, к структуральному повреждению миокарда и к развитию токсической кардиомиопатии и миокардита.
Следует признать, что клинически значимое удлинение интервала QT является грозным, но редким осложнением психотропной терапии (8-10% при лечении антипсихотиками). По-видимому, речь идет о латентной, скрытой форме врожденного СУИ QT с клинической манифестацией вследствие лекарственной агрессии. Интересна гипотеза о дозозависимом характере воздействия препарата на сердечно-сосудистую систему, согласно которой для каждого антипсихотика существует своя пороговая доза, превышение которой и приводит к удлинению интервала QT. Считается, что для тиоридазина это 10 мг/сутки, для пимозида — 20мг/сутки, для галоперидола – 30мг/сутки, для дроперидола – 50мг/сутки, для хлорпромазина – 2000мг/сутки. Высказывается предположение, что удлинение интервала QT также может быть связано с электролитными нарушениями (гипокалиемией).
еет значение и способ введения препарата.
Положение усугубляется сложным коморбидным церебральным фоном психически больных, который сам по себе способен вызывать СУИ QT. Необходимо также помнить, что психически больные получают препараты годами и десятилетиями, а метаболизм подавляющего большинства психотропных средств осуществляется в печени, с участием системы цитохрома Р450.
Цитохром Р450: лекарства, метаболизируемые определенными изомерами (по Pollock B.G. et al., 1999)
Выделяют 4 статуса генетически детерминированного метаболического фенотипа:
o экстенсивные (быстрые) метаболизанты (Extensive Metabolizers или fast) – имеющие две активные формы энзимов микросомального окисления; в терапевтическом плане – это пациенты стандартных терапевтических доз.
o промежуточные метаболизанты (Intermediate Metabolizers) — имеющие одну активную форму энзима и вследствие этого несколько сниженный лекарственный метаболизм
o низкие метаболизанты или медленные (Poor Metabolizers или slow) – не имеющие активных форм энзимов, вследствие чего концентрация препарата в плазме крови может возрастать в 5-10 раз
o сверхинтенсивные метаболизанты (Ultra-extensive Metabolizers) – имеющие три и более активных форм энзимов и ускоренный лекарственный метаболизм
Многие психотропные препараты (особенно нейролептики, производные фенотиазина) оказывают гепатотоксическое действие (вплоть до развития холестатической желтухи), обусловленное комплексным (физико-химическим, аутоиммунным и прямым токсическим) воздействием на печень, что в ряде случаев может трансформироваться в хроническое поражение печени с нарушением ферментного метаболизма по типу «poor metabolizing» («бедного» метаболизма).
Кроме того, многие нейротропные препараты (седативные, антиконвульсанты, нейролептики и антидепрессанты) являются ингибиторами микросомального окисления системы цитохрома Р450, главным образом, энзимов 2С9, 2С19, 2D6, 1A2, 3A4, 5, 7.
Лекарственные средства, приводящие к блокированию изоэнзима CYP 3A4 системы цитохрома Р450. (A.John Camm, 2002).
Ингибиторы 1А
Ингибиторы 2С9
Ингибиторы 2С19
Ингибиторы 2D6
Таким образом, создаются предпосылки для кардиоваскулярных осложнений при неменяющейся дозе психотропного препарата и при неблагоприятных лекарственных комбинациях.
Выделяют группу высокого индивидуального риска кардиоваскулярных осложнений при лечении психотропными препаратами.
Это пациенты пожилого и детского возраста, с сопутствующей сердечно-сосудистой патологией (заболевания сердца, аритмии, брадикардия менее 50 ударов в минуту), с генетическими повреждениями ионных каналов сердца (врождённый, в т.ч. латентный, и приобретённый СУИ QT), с электролитным дисбалансом (гипокалиемия, гипокальциемия, гипомагнеземия, гипоцинкемия), с низким уровнем метаболизма (“poor”,”slow”- metabolizers), с дисфункцией автономной нервной системы, с выраженными нарушениями функции печени и почек, получающие одновременно препараты, удлиняющие интервал QT, и/или ингибирующие цитохром P450. В исследовании Reilly (2000) факторами риска удлинения интервала QT признаны:
Перед современным врачом стоят сложные задачи правильного выбора препарата из огромного количества лекарств (в России это 17 000 наименований!) по критериям эффективности и безопасности.
Грамотное мониторирование интервала QT позволит избежать серьезных кардиоваскулярных осложнений психотропной терапии.
Литература
1.Buckley NA and Sanders P. Cardiovascular adverse effects of antipsychotic drugs / Drug Safety 2000;23(3):215-228
2.Brown S. Excess mortality of schizophrenia, a meta-analysis./ Br J Psychiatry 1997;171:502-508
3.O’Brien P and Oyebode F. Psychotropic medication and the heart. / Advances in Psychiatric Treatment. 2003;9:414-423
4.Abdelmawla N and Mitchel AJ. Sudden cardiac death and antipsychotics drugs. / Advances in Psychiatric Treatment 2006;12:35-44;100-109
5.Herxheimer A, Healy D. Arrythmias and sudden death in patients taking antipsychotic drugs./ BMI 2002; 325:1253-1254
6.FDA issues public health advisory for antipsychotic drugs used for treatment of behavioral disorders in elderly patients (FDA talk Paper) Rochvill (MD): US Food and Drug Adminstration,2006
7.Schwartz PJ. The Long QT Syndrome. / Vol.7, Futura Publishing Company, Inc., Armonk, NY, 1997
8.Schwartz PJ, Spazzolini C, Crotti L et al The Jervell and Lange-Nielsen Sundrome: natural history, molecular basis and clinical outcome. / Circulation 2006;113:783-790
9.Бутаев Т.Д., Трешкур Т.В., Овечкина М.А., Порядина И.И., Пармон Е.В. /Врождённый и приобретённый синдром удлинённог интервала QT (учебно-методическое пособие) Инкарт.Санкт-Петербург, 2002
10.Camm AJ. Drug-Induced Long QT Syndrome / Vol.16, Futura Publishing Company, Inc., Armonk, NY, 2002
11.van de Kraats GB, Slob J, Tenback DE. ./ Tijdschr Psychiatr 2007;49(1):43-47
12.Glassman AH and Bigger JR. Antipsychotic drugs: prolonged QTc interval, torsade de pointes and sudden death./ American Journal of Psychiatry 2001;158:1774-1782
13.Vieweg WVR. Neu-generation antipsychotic drugs and QTc-interval prolongation./ Primary Care Companion J Clin Psychiatry 2003;5:205-215
14.Mehtonen OP, Aranki K, Malkonen L et al. A survey of sudden death associated with the use of antipsychotics or antidepressant drugs: 49 cases in Finland./ Acta Psychiatrica Scandinavica 1991;84:58-64
15.Ray WA, Meredith S, Thapa PB et al. Antipsychotics and the risk of sudden cardiac death./ Archives of General Psychiatry 2001;58:1161-1167
16.Straus SMJM, Bleumink GS, Dieleman JP et al. Antipsychotics and the risk of sudden cardiac death./ Archives of Internal Medicine 2004;164:1293-1297
17.Trenton AJ, Currier GW, Zwemer FL. Fatalities associated with therapeutic use and overdose of atypical antipsychotics / CNS Drugs 2003;17:307-324
18.Victor W and Wood M. Tricyclic Antidepressants, QT Interval and Torsade de Pointes./ Psychosomatics 2004;45:371-377
19.Thorstrand C. Clinical features in poisoning by tricyclic antidepressants with special reference to the ECG./ Acta Med Scan 1976;199:337-344
20.Wilens TE, Biederman J, Baldessarini RJ et al. Cardiovascular effects of therapeutic doses of tricyclic antidepressants in children and adolescents./ J Am Acad Child Adolesc Psychiatry 1995;35:1474-1480
21. Riddle MA, Geller B, Ryan N. Another sudden death in a child treated with desipramine./ J Am Acad Child Adolesc Psychiatry 1993;32:792-797
22.Varley CK, McClellan J. Case study: two additional sudden deaths with tricyclic antidepressants./ J Am Acad Child Adolesc Psychiatry 1997;36:390-394
23.Oesterheld J. TCA cardiotoxicity: the latest./ J Am Acad Child Adolesc Psychiatry 1996;34:1460-1468
24.Swanson JR, Jones GR, Krasselt W et al. Death of two subjects due to imipramine and desipramine metabolite accumulation during chronic therapy: a review of the literature and possible mechanisms./ J Forensic Sci 1997;42:335-339
25.Haverkamp W, Breithardt G, Camm AJ et al. The potential for QT prolongation and proarrhythmia by non-antiarrhythmic drugs: clinical and regulatory implications. Report on a policy conference of the European Society of Cardiology / Eur Heart J 2000;21(5):1216-1231
26.Ogata N, Narahashi T. Block of sodium channels by psychotropic drugs in single quinea-pig cardiac myocytes / Br J Pharmacol 1989;97(3):905-913
27.Crumb WJ, Beasley C, Thornton A et al. Cardiac ion channel blocking profile of olanzapine and other antipsychotics. Presented at the 38th American College of Neuropsychopharmacology Annual Meeting; Acapulco, Mexico; December 12-16,1999
28.Jo SH, Youm JB, Lee CO et al. Blocade of the HERG human cardiac K+channel by the antidepressant drug amitriptyline./ Br J Pharmacol 2000;129:1474-1480
29.Kupriyanov VV, Xiang B, Yang L, Deslauriers R./ Lithium ion as a probe of Na+channel activity in isolated rat hearts: a multinuclear NMR study./ NMR Biomed 1997;10:271-276
30.Kiesecker C, Alter M, Kathofer S et al. Atypical tetracyclic antidepressant maprotiline is an antagonist at cardiac HERG potassium channels./ Naunyn Schmiedebergs Arch Pharmacol 2006;373(3):212-220
31.Tarantino P, Appleton N, Lansdell K. Effect of trazodone on HERGchannel current and QT-interval./ Eur J Pharmacol 2005;510(1-2):75-85
32.Jow F, Tseng E, Maddox T et al. Rb+ efflux through functional activation of cardiac KCNQ1/mink channels by the benzodiazepine R-L3 (L-364,373)./ Assay Drug Dev Technol 2006;4(4):443-450
33.Rajamani S, Eckhardt LL, Valdivia CR et al. Drug-induced long QT syndrome: HERG K+ channel block and disruption of protein trafficking by fluoxetine and norfluoxetine./ Br J Pharmacol 2006;149(5):481-489
34. Glassman AH. Schizophrenia, antipsychotic drugs, and cardiovascular disease./ J Clin Psychiatry 2005;66 Suppl 6:5-10
35.Shamgar L, Ma L, Schmitt N et al. Calmodulin is essential for cardiac IKS channel gating and assembly: impaired function in long-QT mutations./ Circ Res 2006;98(8):1055-1063
36. Hull BE, Lockwood TD. Toxic cardiomyopaty: the effect of antipsychotic-antidepressant drugs and calcium on myocardial protein degradation and structural integrity./ Toxicol Appl Pharmacol 1986;86(2):308-324
37.Reilly JG, Ayis SA, Ferrier IN et al. QTc-interval abnormalties and psychotropic drugs therapy in psychiatric patients./ Lancet 2000;355(9209):1048-1052
38.Andreassen OA, Steen VM. ./ Tidsskr Nor Laegeforen 2006;126(18):2400-2402
39.Kutscher EC, Carnahan R. Common CYP450 interactions with psychiatric medicines: A brief review for the primary care physician./S D Med 2006;59(1):5-9
40.Kropp S, Lichtinghagen R, Winterstein K et al. Cytochrome P450 2D6 and 2C19 polymorphisms and length of hospitalization in psychiatry./ Clin Lab 2006;52(5-6):237-240
41.Daniel WA. The influence of long-term treatment with psychotropic drugs on cytochrome P450: the involvement of different mechanisms./ Expert Opin Drug Metab Toxicol 2005;1(2):203-217
42.Kootstra-Ros JE, Van Weelden MJ, Hinrichs JM et al. Therapeutic drug monitoring of antidepressants and cytochrome P450 genotyping in general practice./ J Clin Pharmacol 2006;46(11):1320-1327 43.Андреев Б.В., Лиманкина И.Н. Проблема интервала QT в психиатрической практике./ Медицина ХХ век 2006;4:41-44
СИНДРОМ УДЛИНЁННОГО ИНТЕРВАЛА QT И ПРОБЛЕМЫ БЕЗОПАСНОСТИ ПСИХОФАРМАКОТЕРАПИИ
© Лиманкина, И. Н.
Санкт-Петербургская психиатрическая больница №1 им. П.П.Кащенко
Частота негативных кардиоваскулярных эффектов психотропной терапии, по данным масштабных клинических исследований, достигает 75% . Психически больные имеют достоверно более высокий риск внезапной смерти . Так, в сравнительном исследовании (Herxheimer A. et Healy D., 2002) показано 2-5-кратное увеличение частоты внезапной смерти у пациентов с шизофренией в сравнении с двумя другими группами (больные глаукомой и псориазом) . Американское агентство по контролю за продуктами питания и лекарствами (USFDA) сообщило об 1,6-1,7-кратном повышении риска внезапной смерти при использовании всех современных антипсихотических препаратов (как классических, так и атипичных) . Одним из предикторов внезапной смерти при терапии психотропными препаратами считают синдром удлинённого интервала QT (CУИ QT) .
Интервал QT отражает электрическую систолу желудочков (время в секундах от начала комплекса QRS до конца зубца Т). Его продолжительность зависит от пола (у женщин QT длиннее), возраста (с возрастом QT удлиняется) и частоты сердечных сокращений (ЧСС) (обратно пропорционально). Для объективной оценки интервала QT в настоящее время пользуются корригированным (с поправкой на ЧСС) интервалом QT (QTc), определяемым по формулам Базетта и Фредерика:
Формула Базетта (Bazett) QTс = QT / RК 1/2
при RR
Формула Фредерика (Friderici) QTс = QT / RR 1/3
при RR >1000 мс
В норме QTc составляет 340-450 мс для женщин и 340-430 мс для мужчин. Известно, что СУИ QT опасен развитием фатальных желудочковых аритмий и фибрилляции желудочков . Риск внезапной смерти при врожденном СУИ QT в отсутствие адекватного лечения достигает 85%, при этом 20% детей умирают в течение года после первой потери сознания и более половины - в первое десятилетие жизни .
В этиопатогенезе заболевания ведущая роль отводится мутациям в генах, кодирующих калиевые и натриевые каналы сердца . В настоящее время идентифицировано 8 генов, ответственных за развитие клинических проявлений СУИ QT (табл. 1). Кроме того доказано, что у больных СУИ QT имеется врожденный симпатический дисбаланс (асимметрия иннервации сердца) с преобладанием левосторонней симпатической иннервации.

В клинической картине заболевания доминируют приступы потери сознания (синкопе), связь которых с эмоциональным (гнев, страх, резкие звуковые раздражители) и физическим стрессом (физическая нагрузка, плавание, бег) подчеркивает важную роль симпатической нервной системы в патогенезе СУИ QT.
Продолжительность потери сознания составляет в среднем 1-2 минуты и в половине случаев сопровождается эпилептиформными, тонико-клоническими судорогами с непроизвольным мочеиспусканием и дефекацией. Поскольку синкопальные состояния могут встречаться и при других заболеваниях, часто таких пациентов трактуют как больных с эпилепсией, истерией.
Особенности синкопальных состояний при СУИ QT:
- как правило, возникают на высоте психоэмоциональной или физической нагрузки;
- типичны предвестники (внезапная общая слабость, потемнение в глазах, сердцебиение, тяжесть за грудиной);
- быстрое, без амнезии и сонливости, восстановление сознания;
- отсутствие изменений личности, характерных для больных эпилепсией.
Синкопальные состояния при СУИ QT обусловлены развитием полиморфной желудочковой тахикардии типа «пируэт» («torsades de pointes») (TdP). TdP называют ещё «сердечным балетом», «хаотической тахикардией», «желудочковой анархией», «сердечным штормом», что по сути является синонимом остановки кровообращения. TdP - неустойчивая тахикардия (общее количество QRS комплексов при каждом приступе колеблется от 6 до 25-100), склонная к рецидивам (уже через несколько секунд или минут приступ может повториться) и переходу в фибрилляцию желудочков (относится к жизнеугрожающим аритмиям). К другим электрофизиологическим механизмам внезапной кардиогенной смерти пациентов с СУИ QT относят электромеханическую диссоциацию и асистолию.
ЭКГ-признаки СУИ QT
- Удлинение интервала QT превышающее норму для данной ЧСС более чем на 50 мс, независимо от причин, лежащих в его основе, общепризнанно считается неблагоприятным критерием электрической нестабильности миокарда. Комитет по патентованным лекарственным средствам Европейского Агентства по оценке медицинских продуктов (European Agency for the Evaluation of Medical Products) предлагает следующую интерпретацию продолжительности интервала QTc (табл. 2). Увеличение QTc на 30-60 мс у пациента, принимающего новые лекарственные средства, должно вызывать настороженность в отношении возможной связи с препаратом. Абсолютную продолжительность QTc свыше 500 мс и относительное увеличение более чем на 60 мс следует рассматривать в качестве угрозы TdP.
- Альтернация зубца Т - изменение формы, полярности, амплитуды зубца Т свидетельствует об электрической нестабильности миокарда.
- Дисперсия интервала QT - разница между максимальным и минимальным значением интервала QT в 12 стандартных отведениях ЭКГ. QTd = QTmax - QTmin, в норме QTd = 20-50мс. Увеличение дисперсии интервала QT свидетельствует о готовности миокарда к аритмогенезу.

Отмечаемый в последние 10-15 лет растущий интерес к исследованию приобретенного СУИ QT расширил наши представления о внешних факторах, таких как различные заболевания, метаболические нарушения, электролитный дисбаланс, лекарственная агрессия, вызывающих нарушения функционирования ионных каналов сердца, аналогичные врожденным мутациям при идиопатическом СУИ QТ.
Клинические состояния и заболевания, тесно ассоциированные с удлинением интервала QT представлены в табл. 3.

Согласно данным, приведенным в докладе Центров по контролю и предупреждению заболеваний (Centers for Disease Control and Prevention) от 2.03.2001 г., в США растет частота внезапной сердечной смерти среди людей молодого возраста. Высказывается мнение, что среди возможных причин этого роста важную роль играют лекарственные средства. Объем потребления лекарств в экономически развитых странах постоянно увеличивается. Фармацевтика давно стала таким же бизнесом как и любой другой. Только на разработку нового продукта у фармацевтических гигантов в среднем уходит около 800 млн. долларов, что на два порядка выше, чем в большинстве других областей.
Наметилась отчетливая негативная тенденция в проведении фармкомпаниями все большего числа препаратов как статусных или престижных (lifestyle drugs). Такие лекарства принимают не потому, что они нужны для лечения, а потому что они соответствуют определенному образу жизни. Это Виагра и ее конкуренты Сиалис и Левитра; Ксеникал (средство для снижения веса), антидепрессанты, пробиотики, антигрибковые и многие другие препараты.
Другую тревожную тенденцию можно обозначить как Disease Mongering (торговлю болезнями). Крупнейшие фармкомпании, чтобы расширить рынок сбыта, убеждают вполне здоровых людей в том, что они больны и нуждаются в медикаментозном лечении. Количество мнимых недугов, искусственно раздуваемых до масштабов серьезных заболеваний, постоянно увеличивается. Синдром хронической усталости (синдром менеджера), климакс как заболевание, женская половая дисфункция, иммунодефицитные состояния, йоддефицит, синдром беспокойных ног, дисбактериоз, «новые» инфекционные заболевания становятся брендами для наращивания продаж антидепрессантов, иммуномодуляторов, пробиотиков, гормонов.
Самостоятельный и бесконтрольный прием лекарственных средств, полифармация, неблагоприятные комбинации препаратов и необходимость длительного приема лекарственных средств создают предпосылки для развития СУИ QT. Таким образом, индуцированное лекарствами удлинение интервала QT как предиктор внезапной смерти, приобретает масштабы серьезной медицинской проблемы. Разнообразные лекарственные препараты самых широких фармакологических групп способны приводить к удлинению интервала QT (табл. 4). Список препаратов, удлиняющих интервал QT, постоянно пополняется. Все лекарственные средства центрального действия удлиняют интервал QT, зачастую клинически значимо, и именно поэтому проблема лекарственно-индуцированного СУИ QT в психиатрии стоит наиболее остро .

В серии многочисленных публикаций доказана связь между назначением антипсихотиков (как старых, классических, так и новых, атипичных) и СУИ QT, TdP и внезапной смертью . В Европе и США предоставление лицензии для нескольких нейролептиков не допускали или откладывали, другие были сняты с производства. После сообщений о 13 случаях внезапной необъяснимой смерти, связанной с приёмом пимозида, в 1990 году было принято решение об ограничении его суточной дозы до 20 мг в сутки и лечении под контролем ЭКГ. В 1998 году после публикации данных о связи приёма сертиндола с 13 случаями серьёзной, но не фатальной аритмии (36 смертельных случаев были предположительными) фирма-производитель добровольно временно прекратила продажу препарата на 3 года. В том же году по поводу удлинения интервала QT тиоридазин, мезоридазин и дроперидол получили предостережение в форме «чёрной вставки», а зипразидон - полужирным шрифтом. К концу 2000 года после смерти 21 человека вследствие приёма назначенного врачами тиоридазина, этот препарат стал препаратом второй очереди в лечении шизофрении. Вскоре после этого дроперидол был отозван с рынка его производителями. В Соединённом Королевстве выпуск атипичного антипсихотического препарата зипразидона откладывают, поскольку более чем у 10% пациентов, принимающих этот препарат, возникло лёгкое удлинение интервала QT.
Из антидепрессантов кардиотоксический эффект в наибольшей степени проявляют циклические антидепрессанты . По данным исследования 153 случаев отравления ТЦА (из которых 75% приходилось на амитриптилин) клинически значимое удлинение интервала QTс отмечалось в 42% случаев . Из 730 детей и подростков, получавших антидепрессанты в терапевтических дозах, удлинение интервала QTс > 440 мс сопровождало лечение дезипрамином в 30%, нортриптилином в 17%, имипрамином в 16%, амитриптилином в 11% и кломипрамином в 11% . Описаны случаи внезапной смерти, тесно ассоциированной с СУИ QT, пациентов, длительно получавших трициклические антидепрессанты , в т.ч. с посмертной идентификацией «slow-metabolizer» фенотипа CYP2D6 вследствие кумуляции препарата . Новые циклические и атипичные антидепрессанты более безопасны в отношении кардиоваскулярных осложнений, демонстрируя удлинение интервала QT и TdP лишь при превышении терапевтических доз.
Большинство психотропных препаратов, широко используемых в клинической практике, относятся к классу В (по W.Haverkamp 2001), т.е. на фоне их применения имеется относительно высокий риск возникновения TdP . По данным экспериментов in vitro, in vivo, секционных и клинических исследований антиконвульсанты, антипсихотики, анксиолитики, нормотимики и антидепрессанты способны блокировать быстрые калиевые HERG-каналы, натриевые каналы (вследствие дефекта гена SCN5A) и кальциевые каналы L-типа, вызывая, таким образом, функциональную недостаточность всех каналов сердца .
Кроме того, в формировании СУИ QT принимают участие хорошо известные кардиоваскулярные побочные эффекты психотропных препаратов . Многие транквилизаторы, нейролептики, препараты лития, ТЦА снижают сократимость миокарда, что в редких случаях может привести к развитию застойной сердечной недостаточности. Циклические антидепрессанты способны накапливаться в сердечной мышце, где их концентрация в 100 раз превышает уровень в плазме крови. Многие психотропные препараты являются ингибиторами кальмодулина, что приводит к нарушению регуляции синтеза протеинов миокарда, к структуральному повреждению миокарда и к развитию токсической кардиомиопатии и миокардита .
Следует признать, что клинически значимое удлинение интервала QT является грозным, но редким осложнением психотропной терапии (8-10% при лечении антипсихотиками ). По-видимому, речь идет о латентной, скрытой форме врожденного СУИ QT с клинической манифестацией вследствие лекарственной агрессии. Интересна гипотеза о дозозависимом характере воздействия препарата на сердечно-сосудистую систему, согласно которой для каждого антипсихотика существует своя пороговая доза, превышение которой и приводит к удлинению интервала QT. Считается, что для тиоридазина это 10 мг/сутки, для пимозида - 20 мг/сутки, для галоперидола - 30 мг/сутки, для дроперидола - 50 мг/сутки, для хлорпромазина - 2000 мг/сутки. Высказывается предположение, что удлинение интервала QT также может быть связано с электролитными нарушениями (гипокалиемией). Имеет значение и способ введения препарата.
Положение усугубляется сложным коморбидным церебральным фоном психически больных, который сам по себе способен вызывать СУИ QT. Необходимо также помнить, что психически больные получают препараты годами и десятилетиями, а метаболизм подавляющего большинства психотропных средств осуществляется в печени, с участием системы цитохрома Р450 . Лекарства, метаболизируемые определенными изомерами цитохрома Р450 представлены в табл. 5.

Кроме того выделяют 4 статуса генетически детерминированного метаболического фенотипа:
- экстенсивные (быстрые) метаболизанты (Extensive Metabolizers или fast), имеющие две активные формы энзимов микросомального окисления; в терапевтическом плане - это пациенты стандартных терапевтических доз;
- промежуточные метаболизанты (Intermediate Metabolizers), имеющие одну активную форму энзима и вследствие этого несколько сниженный лекарственный метаболизм;
- низкие или медленные метаболизанты (Poor Metabolizers или slow), не имеющие активных форм энзимов, вследствие чего концентрация препарата в плазме крови может возрастать в 5-10 раз;
- сверхинтенсивные метаболизанты (Ultra-extensive Metabolizers), имеющие три и более активных форм энзимов и ускоренный лекарственный метаболизм.
Многие психотропные препараты (особенно нейролептики, производные фенотиазина) оказывают гепатотоксическое действие (вплоть до развития холестатической желтухи), обусловленное комплексным (физико-химическим, аутоиммунным и прямым токсическим) воздействием на печень, что в ряде случаев может трансформироваться в хроническое поражение печени с нарушением ферментного метаболизма по типу «poor metabolizing» («бедного» метаболизма). Кроме того, многие нейротропные препараты (седативные, антиконвульсанты, нейролептики и антидепрессанты) являются ингибиторами микросомального окисления системы цитохрома Р450, главным образом, энзимов 2С9, 2С19, 2D6, 1A2, 3A4, 5, 7. Таким образом, создаются предпосылки для кардиоваскулярных осложнений при неменяющейся дозе психотропного препарата и при неблагоприятных лекарственных комбинациях.
Выделяют группу высокого индивидуального риска кардиоваскулярных осложнений при лечении психотропными препаратами. Это пациенты пожилого и детского возраста, с сопутствующей сердечно-сосудистой патологией (заболевания сердца, аритмии, брадикардия менее 50 ударов в минуту), с генетическими повреждениями ионных каналов сердца (врождённый, в том числе латентный, и приобретённый СУИ QT), с электролитным дисбалансом (гипокалиемия, гипокальциемия, гипомагнеземия, гипоцинкемия), с низким уровнем метаболизма («poor», «slow» metabolizers), с дисфункцией автономной нервной системы, с выраженными нарушениями функции печени и почек, получающие одновременно препараты, удлиняющие интервал QT, и/или ингибирующие цитохром P450. В исследовании Reilly (2000) факторами риска удлинения интервала QT признаны возраст старше 65 лет (относительный риск, ОР=3,0), использование диуретиков (ОР=3,0), галоперидола (ОР=3,6), ТЦА (ОР=4,4), тиоридазина (ОР=5,4), дроперидола (ОР=6,7), высоких (ОР=5,3) и очень высоких доз нейролептиков (ОР=8,2).
Перед современным врачом стоят сложные задачи правильного выбора препарата из огромного количества лекарств (в России это 17 000 наименований!) по критериям эффективности и безопасности. Грамотное мониторирование интервала QT позволит избежать серьезных кардиоваскулярных осложнений психотропной терапии .
Литература
- Buckley N, Sanders P. Cardiovascular adverse effects of antipsychotic drugs // Drug Safety 2000;23(3):215-228
- Brown S. Excess mortality of schizophrenia, a meta-analysis.// Br J Psychiatry 1997;171:502-508
- O’Brien P and Oyebode F. Psychotropic medication and the heart. // Advances in Psychiatric Treatment. 2003;9:414-423
- Abdelmawla N and Mitchel AJ. Sudden cardiac death and antipsychotics drugs. // Advances in Psychiatric Treatment 2006;12:35-44;100-109
- Herxheimer A, Healy D. Arrythmias and sudden death in patients taking antipsychotic drugs.// BMI 2002; 325:1253-1254
- FDA issues public health advisory for antipsychotic drugs used for treatment of behavioral disorders in elderly patients (FDA talk Paper) Rochvill (MD): US Food and Drug Adminstration,2006
- Schwartz PJ. The Long QT Syndrome. // Vol.7, Futura Publishing Company, Inc., Armonk, NY, 1997
- Schwartz PJ, Spazzolini C, Crotti L et al The Jervell and Lange-Nielsen Sundrome: natural history, molecular basis and clinical outcome. // Circulation 2006;113:783-790
- Бутаев Т.Д., Трешкур Т.В., Овечкина М.А. и др. Врождённый и приобретённый синдром удлинённог интервала QT (учебно-методическое пособие) Инкарт.Санкт-Петербург, 2002
- Camm AJ. Drug-Induced Long QT Syndrome // Vol.16, Futura Publishing Company, Inc., Armonk, NY, 2002
- Van de Kraats GB, Slob J, Tenback DE. .// Tijdschr Psychiatr 2007;49(1):43-47
- Glassman AH and Bigger JR. Antipsychotic drugs: prolonged QTc interval, torsade de pointes and sudden death.// American Journal of Psychiatry 2001;158:1774-1782
- Vieweg WVR. Neu-generation antipsychotic drugs and QTc-interval prolongation.// Primary Care Companion J Clin Psychiatry 2003;5:205-215
- Mehtonen OP, Aranki K, Malkonen L et al. A survey of sudden death associated with the use of antipsychotics or antidepressant drugs: 49 cases in Finland.// Acta Psychiatrica Scandinavica 1991;84:58-64
- Ray WA, Meredith S, Thapa PB et al. Antipsychotics and the risk of sudden cardiac death.// Archives of General Psychiatry 2001;58:1161-1167
- Straus SMJM, Bleumink GS, Dieleman JP et al. Antipsychotics and the risk of sudden cardiac death.// Archives of Internal Medicine 2004;164:1293-1297
- Trenton AJ, Currier GW, Zwemer FL. Fatalities associated with therapeutic use and overdose of atypical antipsychotics // CNS Drugs 2003;17:307-324
- Victor W, Wood M. Tricyclic Antidepressants, QT Interval and Torsade de Pointes.// Psychosomatics 2004;45:371-377
- Thorstrand C. Clinical features in poisoning by tricyclic antidepressants with special reference to the ECG.// Acta Med Scan 1976;199:337-344
- Wilens TE, Biederman J, Baldessarini RJ et al. Cardiovascular effects of therapeutic doses of tricyclic antidepressants in children and adolescents.// J Am Acad Child Adolesc Psychiatry 1995;35:1474-1480
- Riddle MA, Geller B, Ryan N. Another sudden death in a child treated with desipramine.// J Am Acad Child Adolesc Psychiatry 1993;32:792-797
- Varley CK, McClellan J. Case study: two additional sudden deaths with tricyclic antidepressants.// J Am Acad Child Adolesc Psychiatry 1997;36:390-394
- Oesterheld J. TCA cardiotoxicity: the latest.// J Am Acad Child Adolesc Psychiatry 1996;34:1460-1468
- Swanson JR, Jones GR, Krasselt W et al. Death of two subjects due to imipramine and desipramine metabolite accumulation during chronic therapy: a review of the literature and possible mechanisms.// J Forensic Sci 1997;42:335-339
- Haverkamp W, Breithardt G, Camm AJ et al. The potential for QT prolongation and proarrhythmia by non-antiarrhythmic drugs: clinical and regulatory implications. Report on a policy conference of the European Society of Cardiology // Eur Heart J 2000;21(5):1216-1231
- Ogata N, Narahashi T. Block of sodium channels by psychotropic drugs in single quinea-pig cardiac myocytes // Br J Pharmacol 1989;97(3):905-913
- Crumb WJ, Beasley C, Thornton A et al. Cardiac ion channel blocking profile of olanzapine and other antipsychotics. Presented at the 38th American College of Neuropsychopharmacology Annual Meeting; Acapulco, Mexico; December 12-16,1999
- Jo SH, Youm JB, Lee CO et al. Blocade of the HERG human cardiac K+channel by the antidepressant drug amitriptyline.// Br J Pharmacol 2000;129:1474-1480
- Kupriyanov VV, Xiang B, Yang L, Deslauriers R. Lithium ion as a probe of Na+channel activity in isolated rat hearts: a multinuclear NMR study.// NMR Biomed 1997;10:271-276
- Kiesecker C, Alter M, Kathofer S et al. Atypical tetracyclic antidepressant maprotiline is an antagonist at cardiac HERG potassium channels.// Naunyn Schmiedebergs Arch Pharmacol 2006;373(3):212-220
- Tarantino P, Appleton N, Lansdell K. Effect of trazodone on HERGchannel current and QT-interval.// Eur J Pharmacol 2005;510(1-2):75-85
- Jow F, Tseng E, Maddox T et al. Rb+ efflux through functional activation of cardiac KCNQ1/mink channels by the benzodiazepine R-L3 (L-364,373).// Assay Drug Dev Technol 2006;4(4):443-450
- Rajamani S, Eckhardt LL, Valdivia CR et al. Drug-induced long QT syndrome: HERG K+ channel block and disruption of protein trafficking by fluoxetine and norfluoxetine.// Br J Pharmacol 2006;149(5):481-489
- Glassman AH. Schizophrenia, antipsychotic drugs, and cardiovascular disease.// J Clin Psychiatry 2005;66 Suppl 6:5-10
- Shamgar L, Ma L, Schmitt N et al. Calmodulin is essential for cardiac IKS channel gating and assembly: impaired function in long-QT mutations.// Circ Res 2006;98(8):1055-1063
- Hull BE, Lockwood TD. Toxic cardiomyopaty: the effect of antipsychotic-antidepressant drugs and calcium on myocardial protein degradation and structural integrity.// Toxicol Appl Pharmacol 1986;86(2):308-324
- Reilly JG, Ayis SA, Ferrier IN et al. QTc-interval abnormalties and psychotropic drugs therapy in psychiatric patients.// Lancet 2000;355(9209):1048-1052
- Andreassen OA, Steen VM. .// Tidsskr Nor Laegeforen 2006;126(18):2400-2402
- Kutscher EC, Carnahan R. Common CYP450 interactions with psychiatric medicines: A brief review for the primary care physician.//S D Med 2006;59(1):5-9
- Kropp S, Lichtinghagen R, Winterstein K et al. Cytochrome P450 2D6 and 2C19 polymorphisms and length of hospitalization in psychiatry.// Clin Lab 2006;52(5-6):237-240
- Daniel WA. The influence of long-term treatment with psychotropic drugs on cytochrome P450: the involvement of different mechanisms.// Expert Opin Drug Metab Toxicol 2005;1(2):203-217
- Kootstra-Ros JE, Van Weelden MJ, Hinrichs JM et al. Therapeutic drug monitoring of antidepressants and cytochrome P450 genotyping in general practice.// J Clin Pharmacol 2006;46(11):1320-1327